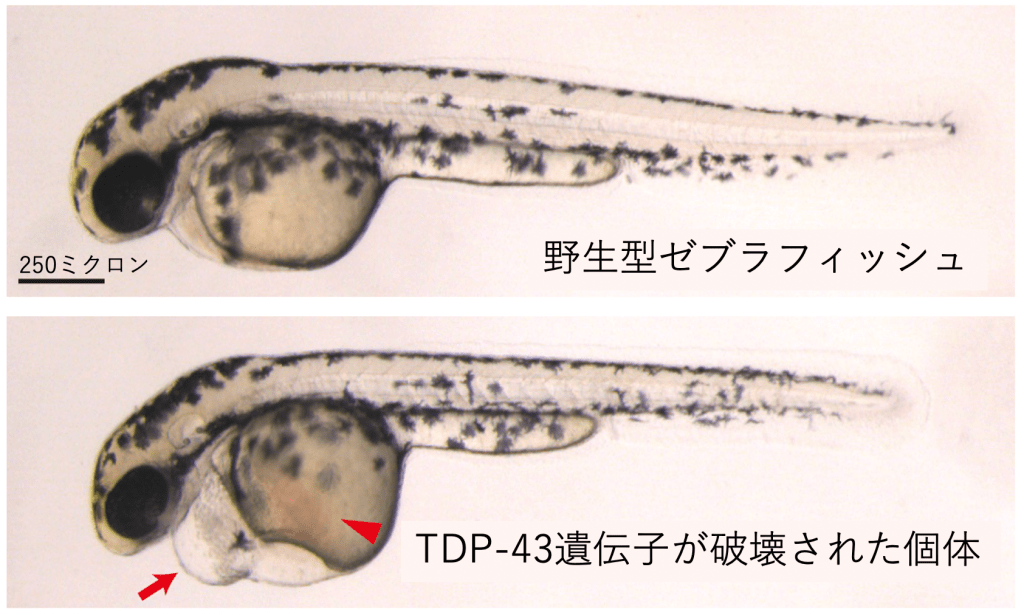
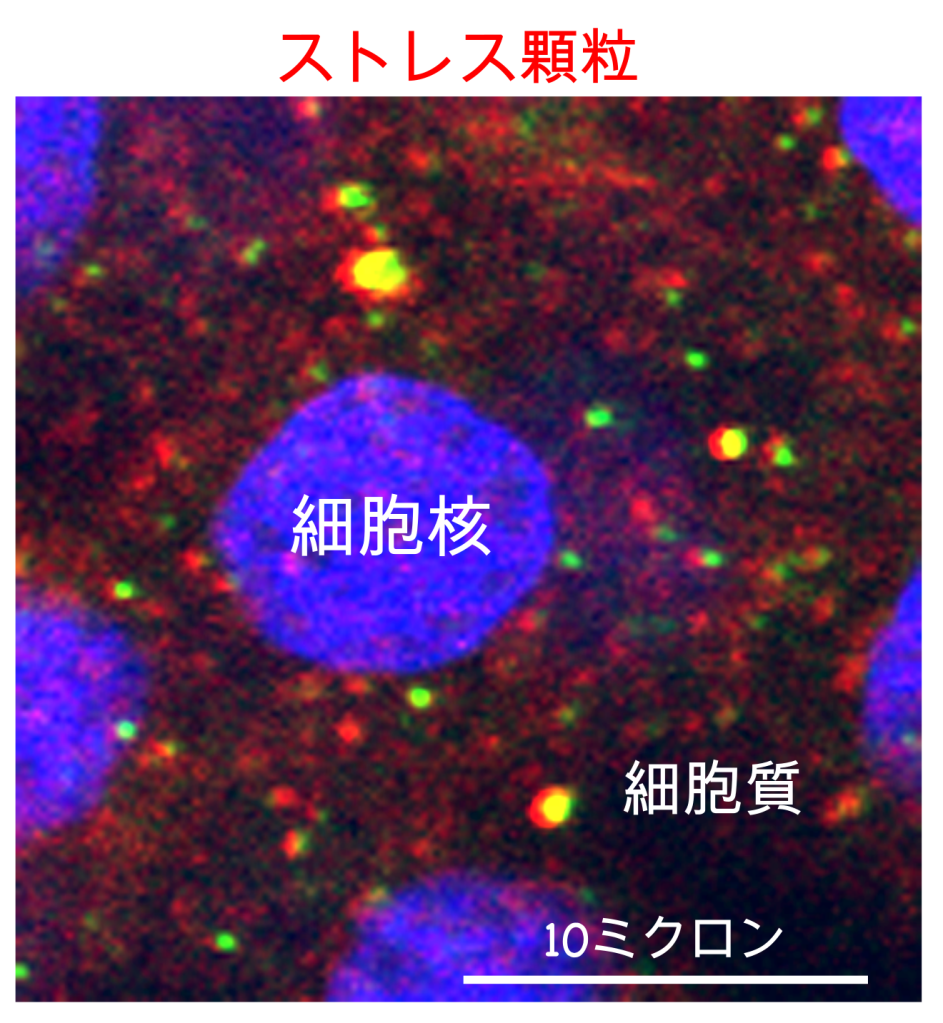
筋萎縮性側索硬化症(ALS)の9割以上を占める、遺伝しないタイプのALS(孤発性ALS)では、形や機能が失われつつある運動ニューロンに溜まる物質の塊が、TDP-43タンパク質を主な成分として含んでいることが、今から15年前に発見されました。
一方で、ALSでは、運動ニューロン以外の脳の神経細胞でも、TDP-43の塊が検出されることがある、とその後報告されています。つまり、ALSでは、運動ニューロンだけでなく、他の神経細胞においてもTDP-43の変化が起こっているのです。
確かに、「形や機能が失われつつある運動ニューロンにTDP-43の塊が溜まる」と聞けば、TDP-43の塊が原因となって、運動ニューロンが障害をうける、という可能性が考えられます。しかし、ALSで比較的障害を受けにくいとされている脳の領域にも、TDP-43の塊が溜まっているのなら、TDP-43の塊が、本当に運動ニューロンに障害を与えているか?という疑問も湧いてきます。
この問題は、いまだ決着がついていない重要な問題です。マウスなどのモデル動物をつかった研究でも、TDP-43を実験的に操作して運動ニューロンが障害を受ける時に、必ずしも、TDP-43の塊が検出されない、という例がいくつか報告されています。
これらの研究成果を総合すると、どうやら、多くのALSでは、TDP-43に変化を与えるような“何らかの異変”が脳や脊髄の多様な細胞で起こっていると予想できます。また、運動ニューロンは、そのような“異変”に対して、相対的にダメージを受けやすい(脆弱、ぜいじゃく、な)個性を持っている可能性が考えられます。このような個性は、神経細胞のALS脆弱性と呼ばれています。
ALS脆弱性をもたらす運動ニューロンの個性について、その実態は未だ明らかではありませんが、候補となるものを、何回かに分けていくつか紹介したいと思います。
まず、運動ニューロンの大きな個性の一つは、大きい細胞サイズ、です。運動ニューロンの最も重要な役割は、脳から送られてきた電気信号を、遠くはなれた筋肉に伝達して、筋肉の伸び縮みをコントロールすることです。だから、細胞が細長くて、体積も大きいのです。
電気信号を正確に送るために、脳からの電気信号がきていない時は、運動ニューロンの細胞膜の電位を一定に保つ必要があります。脳からの電気信号を受け取って、それを筋肉に伝達するために細胞膜の電位を大きく、速く変化させた後は、またすぐに元の電位に戻さなくてはなりません。このような、膜電位の維持には、膨大なエネルギーが必要とされます。
運動ニューロンのサイズが大きければ大きいほど、細胞の表面積が増え、膜電位の維持に必要とされるエネルギーは、膨れ上がります。また、大きい運動ニューロンは、大きい筋肉をコントロールして、身体の大きな動きを生み出していることが知られています。このような大きい運動ニューロンは、運動ニューロンを抑制する働きをもったニューロンとの接続が少なく、爆発的な神経活動を生み出しやすいことが知られています。ALSでは、大きい運動ニューロンほど障害を受けやすい、という事実と関係するかもしれません。
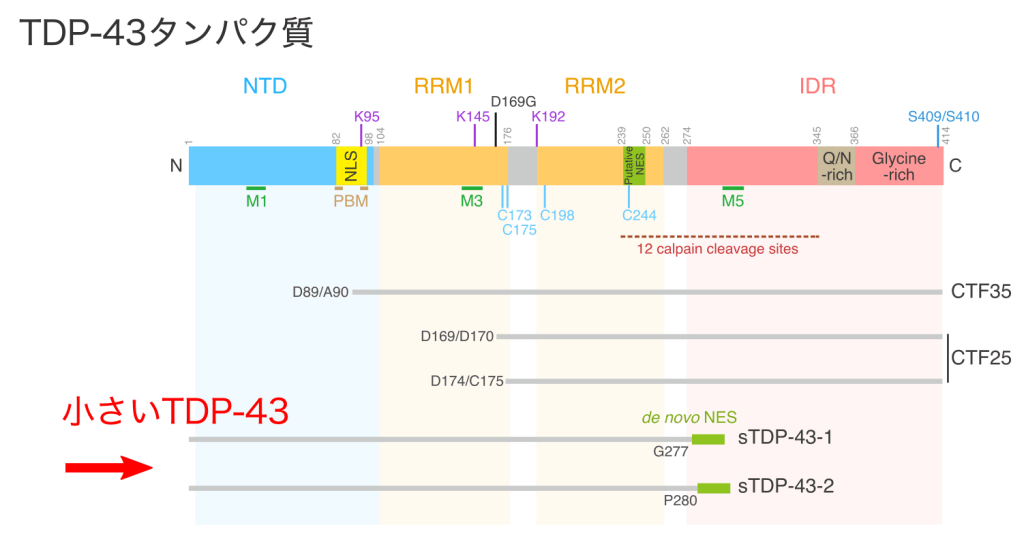
最新の研究で、強く活動している神経細胞では、特殊なTDP-43が生み出されていることが明らかになりました。強い神経活動によって、TDP-43を生み出すためのRNAの配列に変化がおこり、その変化したRNAから作られる、小さめのTDP-43が発見されました。
興味深いことに、この小さいTDP-43は、マウスの運動ニューロンで過剰につくられると、細胞に障害を与え、異常な塊を形成しやすいことがわかってきました。また、この小さいTDP-43をうみだす(と考えられる)RNAは、人間の運動ニューロンにも含まれていることが明らかとなりました。この小さいTDP-43タンパク質の性質を、人間の細胞で詳しく解明する研究が期待されます。
これらの研究がさらに進むことで、強く活動する大きい運動ニューロンほど障害を受けやすく、TDP-43の異常な塊が形成されやすい、というALSの性質を、説明できるようになるかも知れません。
細胞に凍てる雫、TDP−43液滴とALSの接点を探る(13)へ続く
出典