(1)からのつづき
<本文>
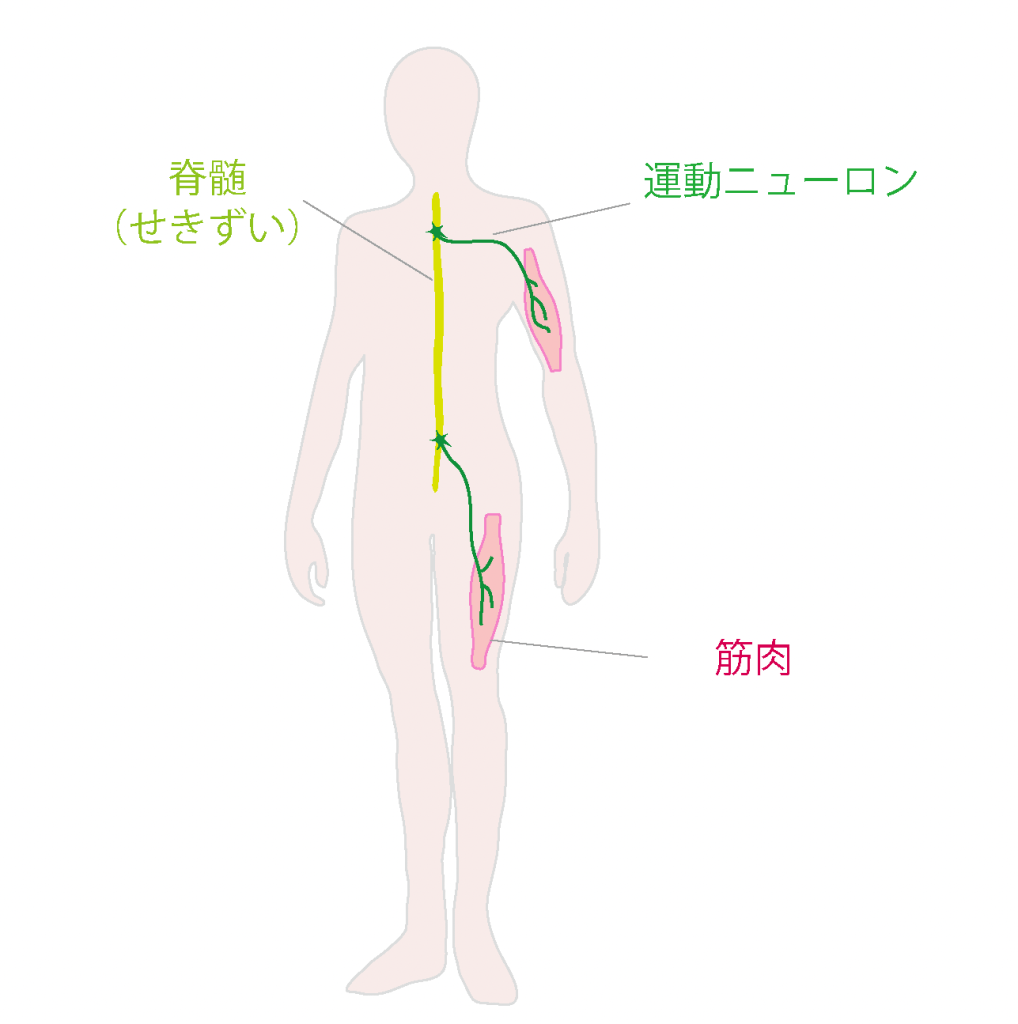
ALSは、筋肉の伸び縮みをコントロールする神経細胞「運動ニューロン」が、徐々に変性する神経の難病です。
運動ニューロンには、背骨の中をとおっている脊髄(せきずい)と筋肉を連結する「下位(かい)運動ニューロン」と、下位運動ニューロンに連結する脳の神経細胞「上位(じょうい)運動ニューロン」があり、ALSではこの両方が変性します。運動ニューロンが変性して筋肉の衰えが進むと、やがては身体を動かすことができなくなります。
9割以上のALSは遺伝しないタイプで、「孤発性(こはつせい)ALS」と呼ばれます。孤発性ALSでは、運動ニューロンにTDP-43と呼ばれるタンパク質が異常な塊として溜まることが知られています。残りの1割は、「家族性ALS」と呼ばれる遺伝するタイプです。家族性ALSのうちの4%では、TDP-43の変異が受け継がれていることが知られています。このことから、TDP-43の変異が原因で、ALSがおこりうることがわかります。しかし、孤発性ALS にはTDP-43の変異がみつからないので、TDP-43変異によっておこる家族性ALSと、孤発性ALSが同じ仕組みでおこるのか、現時点ではわかっていません。
 健康な運動ニューロンとALSの運動ニューロン
健康な運動ニューロンとALSの運動ニューロン
では、TDP-43とは一体何でしょう?
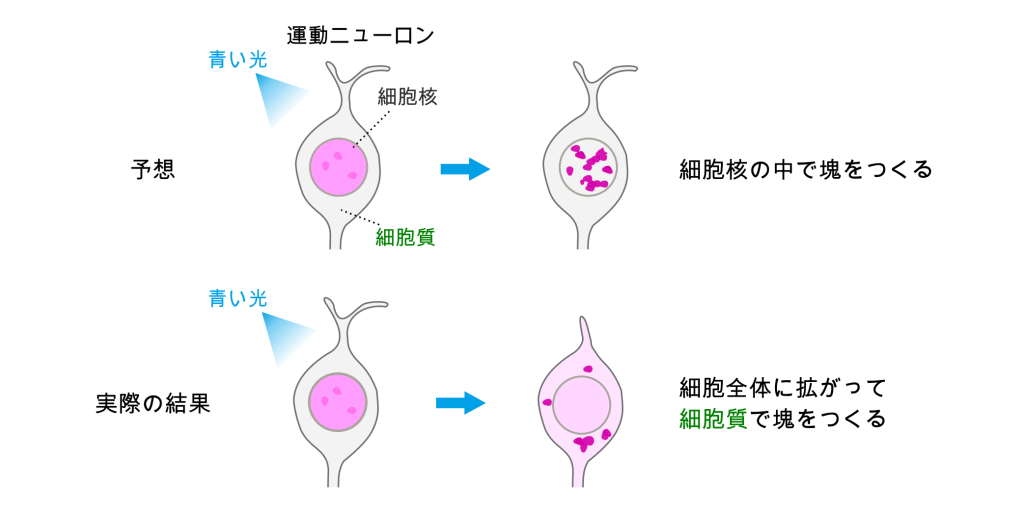
TDP-43は、線虫からヒトまで多くの生き物の体のなかで共通して働いているタンパク質です。例えば、人間の体の中には2万種類の遺伝子があって、それぞれから異なったタンパク質が作られています。TDP-43は、この2万種類のうちの6,000のタンパク質を作りだすために働いていると考えられています。2万種類のタンパク質の設計図ともいうべき遺伝子情報(ゲノム)は、DNAと呼ばれる物質に書き込まれていて、細胞の中では、細胞核(さいぼうかく)とよばれる膜で囲まれた球形の区画に折り畳まれて収納されています(図、左)。健康な細胞では、TDP-43は細胞核に豊富に含まれていて、設計図を書き出してタンパク質を作り出す働きをしています。
ところが、ALSの運動ニューロンでは、TDP-43は細胞核の外に出て、細胞質(さいぼうしつ)と呼ばれる区画で異常な塊になっています(図、右)。健康な時にはTDP-43は細胞核に豊富に含まれていたのに、なぜ、ALSでは細胞質にあるのでしょうか? このTDP-43におこる変化を、人体で観察するよい方法は今のところありません。
この謎を解く為には、まず、健康な細胞でTDP-43がどのように働いているのか?について理解しなくてはなりません。これまでの研究から、TDP-43が以下のような性質を持っていることが明らかになっています。
1)TDP-43は細胞核に豊富だが、細胞核と細胞質を行ったり来たりしている
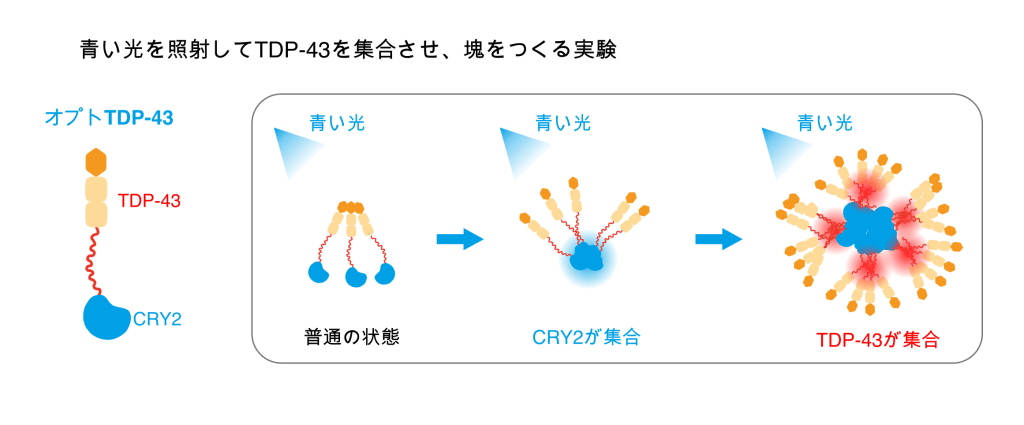
2)いくつかのTDP-43分子が集まることで、TDP-43としての機能がうまれる
3)TDP-43は、細胞質でどんどん分解されている
一般に、タンパク質は、アミノ酸が数珠つなぎになって作られます。タンパク質の材料となるアミノ酸は20 種類あって、アミノ酸をどの順番でいくつつなげるかがDNAの設計図に記されています。TDP-43は、414個のアミノ酸がつながってできています。どうやら、上にあげた3つTDP-43の性質は、414個のアミノ酸の中でも、先頭の100個のアミノ酸のつながりを上手に使うことで生まれている、という証拠が集まってきています。
100個のアミノ酸という小さな領域を、どのように使ったら、このような多彩な性質が生まれるのか、という問題は、現在の最先端の研究課題です。
光遺伝学でALSの謎を照らす(3)につづく
ーーーーーーーー
今年の初めに発表した光遺伝学ALSモデル(Asakawa, 2020)について、まとめとこれからの展望をPerspective記事としてNRR誌に発表しました。記事をもとに、説明を付け加えて和訳しました。
【出典】
Do not curse the darkness of the spinal cord, light TDP-43. Asakawa K, Handa H, Kawakami K (2021) Neural Regen Res 16(5):986-987.