公益財団法人、光科学技術研究振興財団の令和2年度の助成金をいただくことになりました。
コロナ禍の現状を鑑みて、贈呈式は中止となってしまいました。その代わりに、助成金の目録を送ってくださいました。
研究テーマは、「光遺伝学を用いた筋萎縮性側索硬化症(ALS)モデルの開発」です。この支援を活かして、ALS研究を発展させたいと思います。


公益財団法人、光科学技術研究振興財団の令和2年度の助成金をいただくことになりました。
コロナ禍の現状を鑑みて、贈呈式は中止となってしまいました。その代わりに、助成金の目録を送ってくださいました。
研究テーマは、「光遺伝学を用いた筋萎縮性側索硬化症(ALS)モデルの開発」です。この支援を活かして、ALS研究を発展させたいと思います。
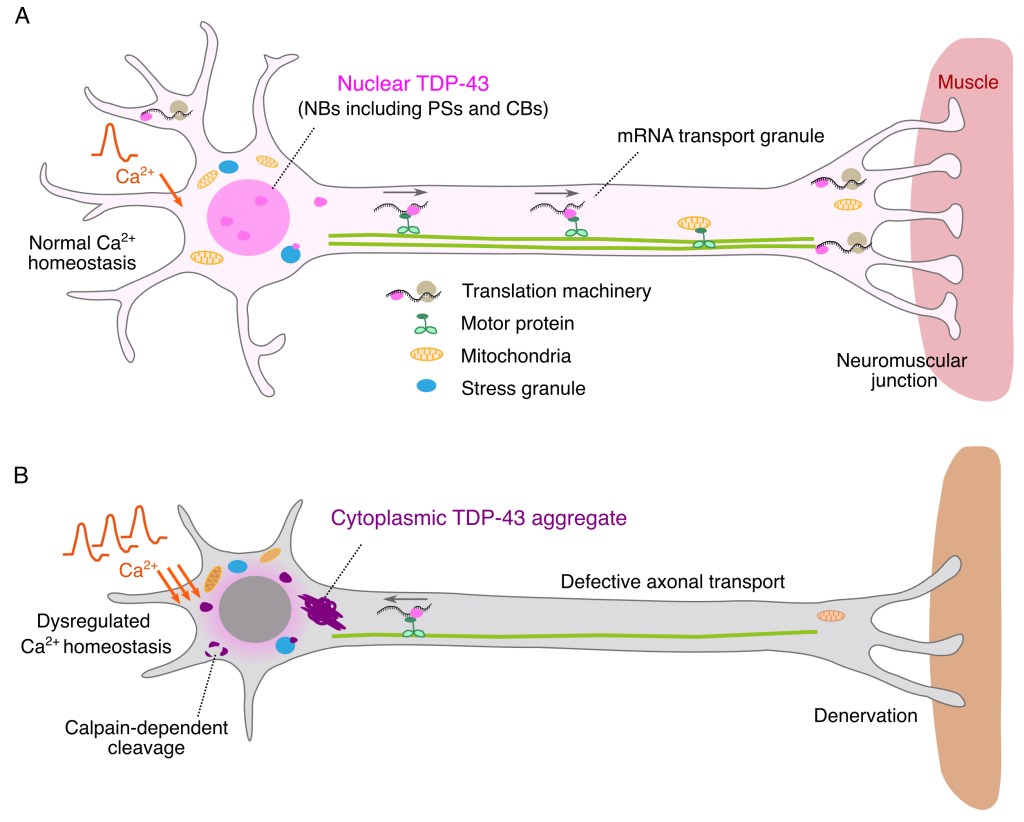
筋萎縮性側索硬化症(ALS)では、意識や五感が保たれたまま、体が動かなくなります。これは、筋肉を収縮させる神経細胞「運動ニューロン」だけが、際立って機能を失うことによります。なぜ、このようなことが起こるのか、未だ謎に包まれています。この現象を、TDP-43と呼ばれるタンパク質の性質から、どのぐらい説明できるのか?について考察した総説を、Cellular and Molecular Life Sciences誌に発表しました。
この総説では、TDP-43に備わっている細胞内で液滴(雫、しずく)をつくる性質に注目します。ALSでは、このTDP-43の雫が、あたかも凍りついてしまったかのように、塊になってしまいます。この現象が、ALSをどのように関わっているのか?このような疑問を抱きながら、和文タイトルは「細胞に凍(い)てる雫、TDP−43液滴とALSの接点を探る」としました。
英文のタイトル、「Multi-phaseted problems of TDP-43 ….」は、TDP-43の機能が多岐にわたっている(Multi-faceted)ことと、TDP−43が、液体から個体の間の様々な状態(相、そう、phase)を行ったり来たりできる性質を持っている(Multi-phase)を合わせた造語です。
できるだけ平易に和訳して、何回かに分けてブログに掲載したいと思います。
Multi-phaseted problems of TDP-43 in selective neuronal vulnerability in ALS
細胞に凍てる雫、TDP−43液滴とALSの接点を探る(1)
要旨
わたしたち人間の体は、およそ2万種類の遺伝子の働きに支えられて、形作られ、機能しています。
この2万種類の遺伝子がもっている遺伝情報を利用して、およそ2万種類のタンパク質が作られますが、その中の一つに、TDP-43(ティー・ディー・ピー・よんじゅうさん)というタンパク質があります。TDP-43は、遺伝情報が書き込まれているDNAや、DNA情報のコピーであるRNA(アールエヌエー)という “DNAの友達”に結合するタンパク質です。人間だけでなく、昆虫、魚、ネズミなど様々な生き物の体の中でも働いているので、生物の進化の中で、保存され受け継がれてきたタンパク質と言えます。
この総説では、このTDP-43タンパク質の働きに注目します。その理由は、このタンパク質が、全身の筋肉が弱って体を動かせなくなってしまう難病、筋萎縮性側索硬化症(きんいしゅくせいそくさくこうかしょう、別名ALS、エイエルエス)の謎を解く鍵になるのではないか、と考えられているからです。ALSで筋肉が弱ってしまうのは、筋肉の伸び縮みのスイッチを押す「運動ニューロン」とよばれる神経細胞が、形や機能をだんだんと失ってしまう(変性する)からです。ALSの原因の多くは今もなお謎のままですが、変性する運動ニューロンに、TDP-43の塊が溜まることが、今から15年前に発見されました。この発見がきっかけとなって、運動ニューロンの中で起こるTDP-43の変化の仕組みを理解できれば、ALSの謎を解くための大切なヒントが得られるののではないか、と期待されるようになりました。
遺伝情報(DNAの配列)が変わることを変異(へんい)と言います。タンパク質は、DNAの配列のコピーであるRNAに書いてある順番にしたがって、アミノ酸を数珠つなぎにしてつくられます。変異が起こると誤った情報を含んだRNAがつくられて、その結果、一部のアミノ酸が入れ替わったタンパク質が作られるようになります。タンパク質の機能に欠かせない大切なアミノ酸が、変異によって入れ替わってしまうと、タンパク質の機能が失われたり、害のあるタンパク質が作られることがあります。このような異常なタンパク質は、多くの病気の原因になっています。一方で、意外なことに、90%以上のALSでは、TDP-43に変異は見当たりません。TDP-43は、健康な細胞の中では、遺伝情報が折り畳まれて収納されている細胞核(さいぼうかく)と呼ばれる膜で囲まれた区画に豊富にあります。しかし、ALSでは、アミノ酸配列は正常なのに、なぜか、TDP-43は細胞核の外側の細胞質(さいぼうしつ)で、塊になってしまうのです。
この問題を解く為には、TDP-43が細胞の中で液滴(ドロップ、専門的には非膜系オルガネラ)をつくる、という性質に着目する必要があるのではないか、と近年は考えられようになっています。例えば、サラダにかけるドレンシングを思い浮かべていただくと、冷蔵庫から取り出したばかりのボトルの中では、油と水が上と下に分かれています。ボトルを激しく振れば、油と水が一見混ざったようにみえます。しかし、よくみると油が無数の小さなドロップ状(しずく状)になって、柔軟に形を変えながら、小さいドロップが合わさって少し大きなドロップになったり、時には、くびり切れてより小さいドロップになったりしているのがわかります。TDP-43も、水の中にある油の如く、ドロップ状になって、別の様々なタンパク質やRNAと結合して、柔軟に姿を変えながら、多彩な働きをしていると予想されています。
この総説では、細胞の中にあるTDP-43を含んだドロップについて、これまで知られているものについて紹介していきたいと思います。そして、このようなTDP-43の性質からALSを眺めることで、「運動ニューロンだけが変性する」というALSの大きな謎に、どのくらい迫ることができそうか?ということを議論したいと思います。
細胞に凍てる雫、TDP−43液滴とALSの接点を探る(2)につづく
出典
今週は、1週間のうちに2編の総説が受理されました。論文はそんなに頻繁に受理されることはないので、珍しいことです。一気に悦びがくるのはもったいない感じもしますが。
この2報の総説は、昨年の春ごろから書き始めたもので、光遺伝学ALSモデルの研究からみえた疑問点と、ゼブラフィッシュを使ったALSモデルについて、どういった視点から一般化できて、将来の研究に繋がられるかをたっぷりと考えることができました。コロナウイルスによる半Stay-at-home状態の時に話が来たので、できるだけ原稿を書こうと引き受けましたが、やはり、論文を書くというのは簡単なことではありません。締め切りをちょっと延ばしてもらったりして、困難がありましたが、いろいろと考えがまとまってよかったです。論文を読めば読むほどに考えが深まり、先人の偉大な努力の積み重ねに、ただただ畏怖の念を覚えました。
近日中に公開されると思います。なんとかこの2編の総説を和訳して、一般の方々にも少しでも伝わるようにしてみたいと思います。
投稿後にデスクトップマックがこわれるというハプニングがあり、アドビ・イラストレーターで描いた図を、ほとんど初めてのInkscapeで描き直さなければならなくなりました。いまでは、だいぶ上達したので、怪我の功名です。
下図は、Inkscapeで描けるようになった図です。

昨年の3月9日に書き始めた総説を、修正して編集者に送り返しました。長い時間がかかっていますが、とても勉強になりました。脱稿が近い、、と思いたい。

原稿から解放された束の間、芥川龍之介の「鼻」を読みました。
鼻が長いお坊さんのお話です。
唇の前に垂れ下がって、弟子に持ち上げていてもらわないと食べないほど、長い鼻です。
お坊さんは、長い鼻がもたらす生活上の困難さの他に、鼻を笑われて傷つく自尊心に悩んでいます。
研究にも、研究が進まない科学的な悩みと、研究が評価されなかったり批判されたりしたときに乱れ動く自尊心からくる悩み。両方あると思います。
今まで深く考えたことはありませんでしたが、「鼻」を読んで、乱れる自尊心の構造、少し理解できた気がします。
科学的な悩みに集中できると思います。
筋肉の収縮をコントロールする神経細胞「運動ニューロン」が、形や機能をだんだんと失って(変性して)、身体を動かせなくなってしまう病気、筋萎縮性側索硬化症(ALS)では、運動ニューロンにTDP-43と呼ばれるタンパク質が塊をつくって溜まることが知られています。この事実が2006年に発見されて以来、TDP-43の塊が発揮する毒性が原因で運動ニューロンが変性すると一説には予想されていますが、この説の検証が待たれています。
我々は、2020年に発表した論文で、青い光を照射すると塊に変化するTDP-43(オプトTDP-43)を開発しました。この新しいアプローチを使って、TDP-43の塊に毒性があるのか否かを検証しました。さて、TDP-43の塊に毒性はあるのでしょうか?
光を使ってタンパク質をコントロールする“光遺伝学”という手法の強みの一つは、タンパク質に起こる変化を、光のON・OFFによって時間的にコントロールできることです。
私たちは、運動ニューロンが観察しやすい熱帯魚「ゼブラフィッシュ」を使って、運動ニューロンにオプトTDP-43を導入して、魚に青い光を照射すると、3時間後には、オプトTDP-43が、細胞核から、細胞核と細胞質を含む細胞全体に広がることを発見しました。

この後、青い光をさらに照射し続けると、やがて数日後には細胞質にオプトTDP-43塊が溜まり始めます。いっぽう、最初の3時間で青色光の照射をストップすると、オプトTDP-43は塊として溜まることなく、再び、照射前のように細胞核に戻ります。もし、オプトTDP-43の塊そのものに毒性が備わっているのならば、3時間の青色光では、運動ニューロンには異常は現れないはずです。そこで、3時間だけ青色光の照射をした後、光照射を止め、その後の運動ニューロンの様子を詳しく調べてみました。
その結果、3時間の青色光照射を経験した運動ニューロンは、その後、成長速度が著しく低下することがわかりました。さらに、筋肉と接続した運動ニューロンに対して、3時間の青色光を照射すると、筋肉との接続が弱まることがわかりました。
この結果は、オプトTDP-43が、塊として溜まるより前に、運動ニューロンにダメージを与えていることを示しています。
塊を作る前に毒性を発揮している、という予想外の結果が出たために、この実験の当初の目的であった、TDP-43の塊そのものに毒性が備わっているのか、という問いの検証にはなりませんでした。以前のブログ、「上流にさかのぼる」では、TDP-43の塊が(1)毒性の源である、という可能性と、(2)毒性を軽減するためにTDP-43を一まとめにして細胞を保護しようとした痕跡である、という可能性を、いずれも肯定も否定もできないことに触れました。我々の、オプトTDP-43を使った実験でも、この問題は解決できませんでした。
ともあれ、この研究によって、これまで予想されていた前の段階で、TDP-43が運動ニューロンにダメージを与えている可能性が高いことがわかりました。これが今回の研究で得られた最も重要な知見の一つです。
ALSの真の原因に迫るためには、TDP-43 が細胞質で塊を作るよりも前の段階、すなわち、細胞質のTDP-43の濃度が上昇する原因を探ることが有効なのではないか、と予想して、現在はその方で研究を展開しています。
さて、このPerspectiveの稿のタイトル「Do not curse the darkness of the spinal cord light TDP-43」は、“暗闇を呪うより、ロウソクを灯そう (Don’t Curse the Darkness, Light a Candle)”、という中国のことわざにちなみました。7回にわたって、できるだけ内容を平易にして書きました。Perspectiveの最後の一文に、今後の期待を込めます。
“The optical inaccessibility of the spinal cord has been and will continue to be a major obstacle to understanding the dynamic nature of TDP-43 in the spinal motor neurons during both healthy and diseased states. We envisage that optogenetic TDP-43 should serve as a candle to overcome the darkness of the spinal cord. ”
“運動ニューロンが、光が到達しにくい脊髄の中にあるということは(つまり、生体内での観察が容易ではないということは)、これまでも、そして、これからも、運動ニューロンの中でのTDP-43のダイナミックな振る舞いを理解することに対する大きな障壁であり続けるでしょう。光遺伝学TDP-43が、この脊髄の闇を克服するロウソクになるのではないかと期待しています。”
結
ーーーーーーーー
今年の初めに発表した光遺伝学ALSモデル(Asakawa, 2020)について、まとめとこれからの展望をPerspective記事としてNRR誌に発表しました。記事をもとに、説明を付け加えて和訳しました。
【出典】
今年もよろしくお願いいたします。平穏で健康な一年を!
